6月21日,我校生物医学工程学院钱海生教授团队联合第一附属医院王华教授团队以及中山大学附属第七医院何裕隆教授团队,在国际著名学术期刊《美国化学会•纳米(ACS Nano)》(IF: 14.588)发表题为《界面工程制备硫锌锰@聚多巴胺空心纳米球用于谷胱甘肽消耗-光热增强化学动力学疗法(Interfacially Engineered ZnxMn1-xS@Polydopamine Hollow Nanospheres for Glutathione Depleting Photothermally Enhanced Chemodynamic Therapy)》的研究成果,提出一种用于联合癌症治疗的高性能和多功能复合纳米结构的替代策略。钱海生教授、何裕隆教授及王华教授为共同通讯作者,我校为第一通讯单位。
基于其固有的理化特性及对肿瘤微环境(tumor microenvironment,TME)的高敏感性,锰基纳米结构驱动的化学动力学疗法(chemodynamic therapy, CDT)已广泛应用于癌症治疗。然而,芬顿(Fenton)或类芬顿(Fenton-like)试剂不可避免地会对正常细胞产生毒性,即使已经开发了一些表面改性策略(包括聚合物包封、人血清白蛋白〔human serum albumin, HSA〕修饰和介孔二氧化硅装饰等)去增强其生物相容性。但这些策略或表现出对肿瘤细胞杀伤功效不足,或不能实质性的改善生物安全性,无法满足实际需要。因此,开发出不仅可以增加纳米药物的生物相容性,还可以显著提高疗效的新型表面改性技术是一项急需解决的难题。
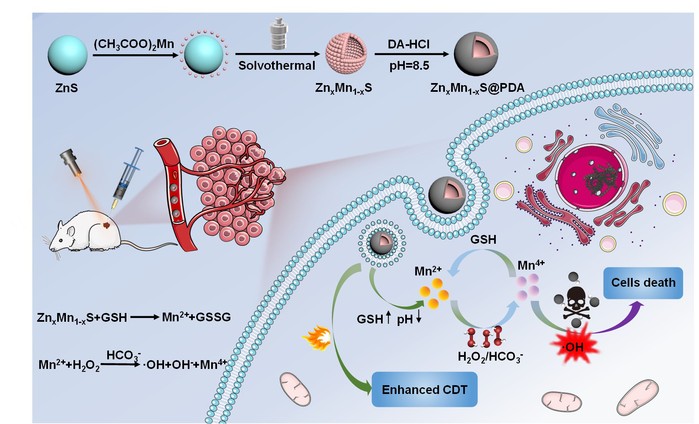
该项研究中,我校教授联合科研团队通过界面工程构建了聚多巴胺(polydopamine, PDA)包覆硫锌锰合金(ZnxMn1-xS@PDA)复合材料。一方面,高价锰离子可消耗肿瘤微环境中过表达的谷胱甘肽(glutathione, GSH),进而降低氧化应激抵制,提高化学动力学疗法疗效;另一方面,通过调节聚多巴胺厚度控制锰离子释放,进而调节锰离子驱动的化学动力学疗法效果,提高硫锌锰合金复合材料的生物相容性,实现其对正常细胞的良好生物相容性和对癌细胞的特异性细胞毒性。此外,聚多巴胺可以提供良好的光热效果以促进化学动力学疗法疗效。
据悉,钱海生教授团队长期致力于肿瘤诊疗材料的设计与开发,这是该团队发展了钆基和铋基等系列肿瘤诊疗纳米生物药物后,再次取得的重要研究成果。(生物医学工程学院)